Por Kleber Karpov
A Universidade de Brasília (UnB) deve desenvolver uma vacina terapêutica in situ com potencial para fortalecer a resposta natural do organismo contra o câncer de mama. A vacina é aplicada diretamente no local do tumor, sem necessidade de preparo prévio em laboratório. A iniciativa é apoiada pela Fundação de Apoio à Pesquisa do Distrito Federal (FAPDF).
O projeto é coordenado pelo professor João Paulo Longo, do Instituto de Ciências Biológicas da UnB. A pesquisa foi premiada no 4º Prêmio FAPDF de Ciência, Tecnologia e Inovação. O dia 27 de novembro, Dia Nacional de Combate ao Câncer, deve reforçar a importância de investir em ciência para ampliar as possibilidades de prevenção, diagnóstico e tratamento.
Inovação baseada em décadas de pesquisa
O projeto deve reunir mais de 20 anos de avanços em nanotecnologia, fototerapia e imunologia tumoral. Estudos anteriores do grupo demonstraram controle de metástases pulmonares em modelos 4T1 , um dos mais agressivos para o estudo do câncer de mama.
Os resultados foram construídos por uma equipe multidisciplinar. Eles já foram publicados em revistas científicas internacionais. Pesquisadores como Camila Magalhães Caradador e Luana Cristina Camargo assinam estudos em periódicos como Current Pharmaceutical Design e Biomedicine & Pharmacotherapy.
As pesquisas mostraram que fármacos como a doxorrubicina, uma quimioterapia capaz de destruir células tumorais, também ativam sinais que estimulam o sistema imunológico. Esse processo, chamado de morte celular imunogênica (MCI), ocorre quando as células cancerígenas liberam moléculas que atraem e ativam células de defesa, funcionando como um alerta natural do organismo.
O entendimento abriu caminho para uma nova abordagem: transformar o próprio tumor em um ponto de ativação da resposta imune. Este é o princípio da vacina terapêutica in situ. Aplicada diretamente no tumor ou ao redor dele, a vacina deve estimular o sistema imunológico dentro do próprio organismo, sem necessidade de preparo prévio em laboratório. O corpo deve reagir aos sinais liberados pelo próprio tumor, tornando o processo mais direto e potencialmente mais aplicável na prática clínica.
O sistema emulgel nanoestruturado
O grupo deve desenvolver um sistema emulgel nanoestruturado. O sistema é um tipo de gel que combina água e óleo na mesma formulação, criando uma base estável capaz de carregar e liberar medicamentos de forma controlada no local aplicado.
Nessa mistura, surfactantes permitem que o gel forme pequenas gotículas estáveis em contato com a água. Essas nanogotículas atuam como veículos para transportar os fármacos. O sistema também incorpora imunoadjuvantes, substâncias que intensificam a resposta do sistema imunológico.
“A grande esperança das imunoterapias é oferecer tratamentos personalizados, menos tóxicos e mais eficazes”, afirmou Longo. “Se conseguirmos resultados semelhantes aos obtidos em laboratório, poderemos estar diante de uma inovação acessível para um grande número de pacientes”.
O professor Longo disse que a estratégia cria “um depósito artificial que libera de forma controlada as moléculas produzidas pela morte celular imunogênica” , favorecendo a ativação de células de defesa. As células dendríticas, monócitos e neutrófilos são essenciais para iniciar a resposta antitumoral.
Como funciona a vacina terapêutica in situ
Na etapa de aplicação, o emulgel deve atuar como um veículo que entrega aos poucos fármacos capazes de induzir a MCI. Fármacos como doxorrubicina, paclitaxel ou mitoxantrona são associados a imunoadjuvantes que reforçam a ativação do sistema imunológico.
A liberação dessas moléculas deve se intensificar com o aumento da temperatura na região, algo comum em processos inflamatórios ao redor do tumor, por ser termossensível.
A MCI envolve três sinais bioquímicos principais:
-
exposição de calreticulina: proteína que migra para a superfície da célula e sinaliza para que seja eliminada;
-
liberação de ATP (adenosina trifosfato): molécula que atua como alerta químico indicando dano;
-
liberação de HMGB1 (High Mobility Group Box 1): proteína que atrai células do sistema imunológico ao local.
Estes sinais são chamados de DAMPs (Padrões Moleculares Associados a Dano), um conjunto de mensagens químicas que avisam ao sistema de defesa que o organismo precisa reagir. O estudo deve seguir um cronograma específico de aplicação das doses e acompanhamento da resposta imunológica para verificar se a vacina é capaz de induzir estes sinais ao longo do tratamento.
Avaliação e resultados esperados
Os resultados da vacinação serão medidos por indicadores como:
-
redução do tumor primário;
-
controle de metástases pulmonares;
-
presença de infiltrado linfocitário, grupo de células de defesa que indica ativação do sistema imunológico.
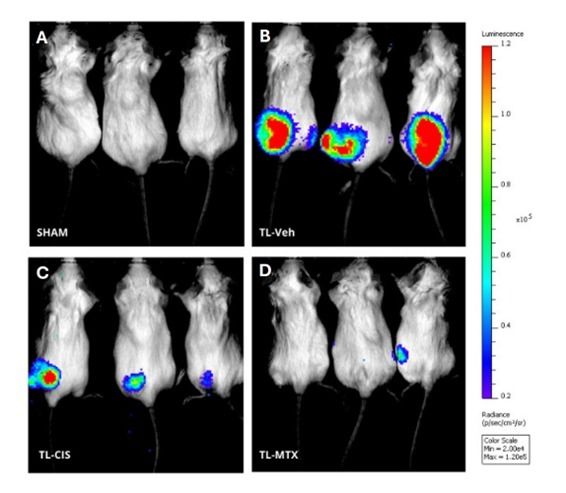
Nos modelos pré-clínicos utilizados, o tumor primário é de mama, mas a disseminação costuma atingir o pulmão. Por isso, este órgão é monitorado como o principal local de metástase durante o estudo.
As análises incluem:
-
tomografia computadorizada;
-
bioluminescência, técnica que utiliza luz emitida por células marcadas para acompanhar a evolução tumoral;
-
imunohistoquímica, método que revela células do sistema imune nos tecidos.
“Durante o estudo pré-clínico, conseguimos rastrear em tempo real como os tumores e as metástases evoluem após a vacinação. Isso nos dá uma visão precisa da eficácia do sistema e do tipo de resposta imunológica que conseguimos induzir”, explicou o professor Longo.
O sistema também é altamente personalizável. Ele permite ajustes nos fármacos e nos componentes conforme o tipo de tumor. A personalização deve ampliar seu potencial para outras neoplasias sólidas.
Desafios e apoio da FAPDF
O desenvolvimento de um sistema nanoestruturado eficaz envolve desafios:
-
garantir a estabilidade da formulação;
-
controlar a liberação dos fármacos;
-
preservar a capacidade imunogênica nos tecidos subcutâneos.
Após os resultados pré-clínicos, uma das próximas etapas é avançar para estudos em pacientes veterinários. A estratégia já foi adotada pelo grupo em outros projetos. Deve contribuir para validações regulatórias e aplicações clínicas futuras.
O professor Longo disse que o apoio da FAPDF tem sido decisivo para a consolidação da pesquisa em nanobiotecnologia e imunologia tumoral no Distrito Federal. “Grande parte dos equipamentos que utilizamos hoje foi adquirida com recursos da FAPDF, incluindo sistemas de imagem e infraestrutura laboratorial. Sem esse apoio, muitos desses estudos simplesmente não existiriam”, destacou.
O presidente da FAPDF, Leonardo Reisman, afirmou que apoiar pesquisas que transformam a vida das pessoas é a essência da Fundação. “Projetos como este mostram que a ciência do Distrito Federal tem capacidade de gerar soluções reais para desafios que impactam milhares de famílias. A inovação não acontece apenas nos grandes centros internacionais — ela acontece aqui, nos nossos laboratórios, pelas mãos de pesquisadores comprometidos com o futuro da saúde brasileira”, disse Leonardo Reisman.
Vacinas terapêuticas baseadas em MCI representam uma das frentes mais promissoras da oncologia contemporânea. Com menor toxicidade e maior personalização, o tipo de abordagem tem potencial para ampliar o acesso a terapias mais seguras, eficazes e humanizadas.
 Kleber Karpov, Fenaj: 10379-DF – IFJ: BR17894
Mestrando em Comunicação Política (Universidade Católica Portuguesa/Lisboa, Portugal); Pós-Graduando em MBA Executivo em Neuromarketing (Unyleya); Pós-Graduado em Auditoria e Gestão de Serviços de Saúde (Unicesp); Extensão em Ciências Políticas por Veduca/ Universidade de São Paulo (USP);Ex-secretário Municipal de Comunicação de Santo Antônio do Descoberto(GO); Foi assessor de imprensa no Senado Federal, Câmara Federal e na Câmara Legislativa do Distrito Federal.
Kleber Karpov, Fenaj: 10379-DF – IFJ: BR17894
Mestrando em Comunicação Política (Universidade Católica Portuguesa/Lisboa, Portugal); Pós-Graduando em MBA Executivo em Neuromarketing (Unyleya); Pós-Graduado em Auditoria e Gestão de Serviços de Saúde (Unicesp); Extensão em Ciências Políticas por Veduca/ Universidade de São Paulo (USP);Ex-secretário Municipal de Comunicação de Santo Antônio do Descoberto(GO); Foi assessor de imprensa no Senado Federal, Câmara Federal e na Câmara Legislativa do Distrito Federal.













